ІНСТРУКЦІЯ
для медичного застосування лікарського засобу
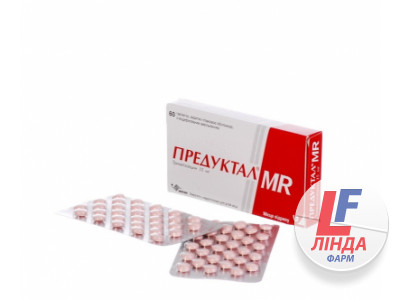
ПРЕДУКТАЛ® MR
(PREDUCTAL® MR)
Склад:
діюча речовина: trimetazidine;
1 таблетка містить: триметазидину дигiдрохлориду 35 мг;
допоміжні речовини:
таблетка: кальцію гiдрофосфату дигiдрат, гiпромелоза 4000, магнію стеарат, повiдон, кремнію діоксид колоїдний безводний;
оболонка: гліцерин, макрогол 6000, магнію стеарат, гiпромелоза, заліза оксид червоний (E 172), титану діоксид (E 171).
Лікарcька форма. Таблетки, вкритi плівковою оболонкою, з модифікованим вивільненням.
Основні фізико-хімічні властивості: рожевого кольору, двоопуклої форми таблетки, вкриті плівковою оболонкою, з тисненням  з одного боку або без тиснення.
з одного боку або без тиснення.
Фармакотерапевтична група. Кардіологічні засоби. Триметазидин. Код АТХ С01Е В15.
Фармакологiчнi властивості.
Фармакодинаміка.
Механізм дії
Завдяки збереженню енергетичного метаболізму у клітинах, які потерпають від гіпоксії або ішемії, триметазидин запобігає зменшенню рівня внутрішньоклітинного АТФ, забезпечуючи тим самим належне функціонування іонних насосів та трансмембранного натрiєво-калiєвого потоку при збереженні клітинного гомеостазу.
Триметазидин інгібує β-окиснення жирних кислот, блокуючи довголанцюгову 3-кетоацил-КоА тiолазу (3-КАТ), що підвищує окиснення глюкози. У клітинах в умовах ішемії процес отримання енергії шляхом окиснення глюкози потребує менше кисню порівняно з процесом отримання енергії шляхом β-окиснення жирних кислот. Посилення процесу окиснення глюкози оптимізує енергетичні процеси у клітинах та відповідно підтримує достатній метаболізм енергії в умовах ішемії.
Фармакодинамічні ефекти
У пацієнтів з ішемічною хворобою серця триметазидин діє як метаболічний агент, зберігаючи внутрішньоклітинні рівні високоенергійних фосфатів у міокарді. Анти-ішемічні ефекти досягаються без супутніх гемодинамічних ефектів.
Клінічна ефективність та безпека
Клінічні дослідження продемонстрували ефективність та безпеку застосування триметазидину для лікування пацієнтів зі стабільною стенокардією як у монотерапії, так і у разі додавання до інших антиангінальних лікарських засобів при їх недостатній ефективності.
Дослідження TRIMPOL-II. Рандомізоване подвійне сліпе плацебо-контрольоване дослі-дження з участю 426 пацієнтів продемонструвало, що додавання триметазидину 60 мг на добу до метопрололу 100 мг (50 мг двічі на добу) протягом 12 тижнів призвело до достовірного покращення показників тестів із навантаженням та покращення клінічних симптомів порівняно з такими при застосуванні плацебо: загальна тривалість навантаження - +20,1 с, p=0,023; загальна виконана робота - +0,54 MET с, p=0,001; час до появи зниження ST-сегмента на 1 мм - +33,4 с, p=0,003; час до виникнення нападу стенокардії - +33,9 с, p<0,001; кількість нападів стенокардії/тиждень - -0,73, p=0,014; застосування нітратів короткої дії/тиждень - -0,63, p=0,032, без зміни показників гемодинаміки.
Дослідження SELLIER. Рандомізоване подвійне сліпе плацебо-контрольоване дослідження з участю 223 пацієнтів продемонструвало, що у підгрупі пацієнтів (n=173), яким додавали триметазидин, таблетки модифікованого вивільнення, по 35 мг (два рази на добу) до 50 мг атенололу (один раз на добу) протягом 8 тижнів, відзначалося достовірне збільшення (+34,4 с, p=0,03) часу до появи зниження ST-сегмента на 1 мм у тестах із навантаженням порівняно з таким при застосуванні плацебо через 12 годин після прийому препарату. Також підтверджено достовірну різницю за показником часу до виникнення нападу стенокардії (p=0,049). За іншими показниками вторинних кінцевих точок між двома групами пацієнтів достовірної різниці виявлено не було (загальна тривалість навантаження, загальна виконана робота та клінічні кінцеві точки).
ДослідженняVASCO. У ході рандомізованого подвійного сліпого дослідження з участю 1962 пацієнтів, яке тривало 3 місяці, до терапії атенололом у дозі 50 мг на добу додавали триметазидин у дозі 70 мг на добу або 140 мг, або плацебо. У загальній популяції, що включала пацієнтів із симптомами та без них, триметазидин не продемонстрував переваг як за ергометричними показниками (загальний час фізичного навантаження, час до появи зниження ST-сегмента на 1 мм та час до виникнення нападу стенокардії), так і за клінічними кінцевими точками. Однак пост-xoк аналіз підгрупи пацієнтів із симптомами (n=1574) показав, що при застосуванні триметазидину у дозі 140 мг на добу спостерігалося достовірне покращення загального часу фізичного навантаження (+23,8 с проти +13,1 с плацебо; p=0,001) та часу до виникнення нападу стенокардії (+46,3 с проти +32,5 с плацебо; p=0,005).
Фармакокінетика.
Максимальна концентрація триметазидину в крові спостерігається в середньому через 5 годин після прийому таблетки. Упродовж доби концентрація у плазмі крові залишається стабільною: протягом 11 годин після прийому таблетки концентрація триметазидину у плазмі крові дорівнює або вища 75 % максимальної концентрації. Стан стабільної концентрації досягається найпізніше на 60-ту годину. Прийом їжі не впливає на фармакокiнетичнi характеристики триметазидину.
Об’єм розподілу становить 4,8 л/кг; зв'язування з білками низьке: за даними вимірювань in vitro – 16 %.
Триметазидин виводиться в основному iз сечею, переважно у незміненій формі. Період напiввиведення становить у середньому 7 годин у здорових молодих добровольців та 12 годин в осіб віком від 65 років. Повне виведення триметазидину є результатом в основному ниркового кліренсу, який безпосередньо корелюється з кліренсом креатиніну, та меншою мірою є результатом печінкового кліренсу, який з віком зменшується.
Особливі групи пацієнтів
Пацієнти літнього віку.
Було проведено спеціальне клінічне дослідження з участю пацієнтів літнього віку з застосуванням триметазидину 35 мг (1 таблетка) 2 рази на добу. Аналіз, проведений кінетичним популяційним методом, показав підвищення концентрації у плазмі крові. У пацієнтів літнього віку можливе підвищення концентрації триметазидину через вікове зниження функції нирок. Спеціальне фармакокінетичне дослідження у пацієнтів віком 75-84 років або ≥ 85 років показало, що у пацієнтів із помірною нирковою недостатністю (кліренс креатиніну 30-60 мл/хв) концентрація триметазидину підвищувалась у 1,0 та 1,3 раза відповідно порівняно з молодшими пацієнтами (віком 30-65 років) із помірною нирковою недостатністю.
Порушення функції нирок. Концентрація триметазидину в крові збільшується в середньому у 1,7 раза у пацієнтів з помірною нирковою недостатністю (кліренс креатиніну - 30‑60 мл/хв) та у 3,1 раза у пацієнтів із тяжкою нирковою недостатністю (кліренс креатиніну < 30 мл/хв) порівняно зі здоровими добровольцями з нормальною функцією нирок. У цій популяції не спостерігалося жодних додаткових занепокоєнь з безпеки порівняно з загальною популяцією.
Клінічні характеристики.
Показання.
Дорослим триметазидин показаний для симптоматичного лікування стабільної стенокардії за умови недостатньої ефективності або непереносимості антиангінальних препаратів першої лінії.
Протипоказання.
- Гіперчутливість до діючої речовини або до будь-якої допоміжної речовини.
- Хвороба Паркінсона, симптоми паркінсонізму, тремор, синдром «неспокійних ніг» та інші рухові розлади, що мають відношення до вищезазначеного.
- Тяжка ниркова недостатність (кліренс креатиніну < 30 мл/хв).
Взаємодія з іншими лікарськими засобами та інші види взаємодій.
Про взаємодію з іншими лікарськими засобами не повідомляли.
Особливості застосування.
Цей лікарській засіб не призначений для купірування нападів стенокардії. Його не слід призначати при нестабільній стенокардії або інфаркті міокарда як первинну терапію на догоспітальному етапі або у перші дні госпіталізації.
У випадку виникнення нападу нестабільної стенокардії на тлі поточної терапії необхідно переглянути стан хвороби пацієнта та відкоригувати лікування (медикаментозну терапію та можливість реваскуляризації).
Триметазидин може спричиняти або погіршувати симптоми паркінсонізму (тремор, акінезія, гіпертонус м’язів), які слід регулярно досліджувати, особливо у пацієнтів літнього віку. У сумнівних випадках пацієнтів потрібно направляти до невропатолога для відповідних обстежень.
При появі рухових розладів, таких як симптоми паркінсонізму, синдрому «неспокійних ніг», тремору, нестійкості ходи, необхідно відмінити триметазидин.
Ці випадки мають низьку частоту виникнення і зазвичай зникають після припинення лікування; у більшості пацієнтів ‒ протягом 4 місяців після припинення прийому триметазидину. Якщо симптоми паркінсонізму зберігаються понад 4 місяці після відміни препарату, необхідно звернутися до невропатолога.
Можуть траплятися падіння, пов'язані з нестійкістю ходи або артеріальною гіпотензією, особливо у пацієнтів, які приймають антигіпертензивне лікування (див. розділ «Побічні реакції»).
Необхідно з обережністю призначати триметазидин пацієнтам з групи ризику підвищення його концентрації:
- пацієнтам з помірною нирковою недостатністю (див. розділ «Спосіб застосування та дози» та «Фармакокінетика»);
- пацієнтам літнього віку від 75 років (див. розділ «Спосіб застосування та дози»).
Застосування у період вагітності або годування груддю.
Вагітність
Дані щодо застосування триметазидину вагітним жінкам відсутні. Дослідження на тваринах не виявили прямого або непрямого небезпечного токсичного впливу на репродуктивну систему. Для запобігання будь-якому ризику застосування триметазидину у період вагітності не рекомендовано.
Годування груддю
Невідомо, чи проникає триметазидин або його метаболіти у грудне молоко. Для запобігання будь-якому ризику для новонароджених/немовлят застосування лікарського засобу ПРЕДУКТАЛ® MR не рекомендовано у період годування груддю.
Здатність впливати на швидкість реакції при керуванні автотранспортом або іншими механізмами.
За даними клінічних досліджень триметазидин не впливає на гемодинаміку, проте у постмаркетинговий період були зафіксовані випадки запаморочення і сонливості (див. розділ «Побічні реакції»), які можуть вплинути на здатність керувати автомобілем і працювати з механізмами.
Спосіб застосування та дози.
Для перорального застосування.
1 таблетка 35 мг триметазидину 2 рази на добу, вранці та ввечері, під час їди.
Після 3 місяців лікування необхідно оцінити результати лікування та у разі відсутності ефекту триметазидин необхідно відмінити.
Особливі групи пацієнтів
Пацієнти з нирковою недостатністю
Пацієнтам із помірною нирковою недостатністю (кліренс креатиніну - 30-60 мл/хв) рекомендована доза становить 1 таблетку на добу вранці під час сніданку (див. розділ «Особливості застосування» та «Фармакокінетика»).
Пацієнти літнього віку
У пацієнтів літнього віку можливе підвищення концентрації триметазидину в крові через вікове зниження функції нирок (див. розділ «Фармакокінетика»). Пацієнтам із помірною нирковою недостатністю (кліренс креатиніну - 30-60 мл/хв) рекомендована доза становить 1 таблетку 35 мг вранці під час сніданку.
Для пацієнтів літнього віку необхідно з обережністю титрувати дозу (див. розділ «Особливості застосування»).
Діти.
Безпеку та ефективність застосування триметазидину дітям (віком до 18 років) не вивчали. Дані відсутні.
Передозування.
Кількість даних щодо передозування триметазидином обмежена. Лікування симптоматичне.
Побічні реакції.
Побічні реакції, що були визначені як побічна дія, яка може бути пов’язана із застосуванням триметазидину, зазначено нижче відповідно до визначеної частоти:
дуже часто (≥ 1/10); часто (≥ 1/100, < 1/10); нечасто (≥ 1/1000, < 1/100); рідко (≥ 1/10000, < 1/1000); дуже рідко (< 1/10000); частота невідома (не може бути визначена згідно з наявною інформацією).
| Класифікація за системами органів | Частота | Побічна реакція |
| З боку нервової системи | Часто | Запаморочення, головний біль |
| Частота невідома | Симптоми паркінсонізму (тремор, акінезія, гіпертонус м’язів), нестійкість ходи, синдром «неспокійних ніг» та інші рухові розлади, що мають відношення до вищезазначеного, які зазвичай минають після припинення лікування |
| Розлади сну (безсоння, сонливість) |
| З боку серця | Рідко | Пальпітація, екстрасистолія, тахікардія |
| З боку судин | Рідко | Артеріальна гіпотензія, ортостатична гіпотензія, яка може бути асоційована з нездужанням, запамороченням або падінням, особливо у пацієнтів, які застосовують антигіпертензивні засоби, почервоніння обличчя |
| З боку травного тракту | Часто | Біль в абдомінальній ділянці живота, діарея, диспепсія, нудота та блювання |
| Частота невідома | Запор |
| З боку шкіри та підшкірної тканини | Часто | Висип, свербіж, кропив’янка |
| Частота невідома | Гострий генералізований екзантематозний пустульоз, ангіоедема |
| Загальні порушення | Часто | Астенія |
| З боку системи крові та лімфатичної системи | Частота невідома | Агранулоцитоз, тромбоцитопенія, тромбоцитопенічна пурпура |
| З боку гепатобіліарної системи | Частота невідома | Гепатит
|
Термін придатності. 3 роки.
Умови зберігання.
Не потребує особливих умов зберігання. Зберігати у недоступному для дітей місці.
Упаковка.
По 30 таблеток у блістері (ПВХ/алюміній); по 2 блістери в коробці з картону.
Категорія відпуску.
За рецептом.
Виробник.
Лабораторії Серв'є Індастрі/Les Laboratoires Servier Industrie.
Місцезнаходження виробника та адреса місця провадження його діяльності.
905 рут де Саран, 45520 Жіді, Франція/905 route de Saran, 45520 Gidy, France.
Виробник.
АНФАРМ Підприємство Фармацевтичне АТ/
ANPHARM Przedsiebiorstwo Farmaceutyczne S.A.
Місцезнаходження виробника та адреса місця провадження його діяльності.
вул. Аннопол 6Б, Варшава, 03-236, Польща/ul. Annopol 6B, Warszawa, 03-236, Poland.
Виробник.
ТОВ «Сердікс»/OOO «Сердикс».
Місцезнаходження виробника та адреса місця провадження його діяльності.
м. Москва, с. Соф’їно, буд. 1/1, 142150, Російська Федерація/
г. Москва, д. Софьино, стр. 1/1, 142150, Российская Федерация.
Заявник.
ТОВ «Серв’є Україна».
Місцезнаходження заявника.
Вулиця Бульварно-Кудрявська, будинок 24, Шевченківський район, м. Київ, 01054, Україна.
У разі виникнення запитань щодо лікарського засобу слід звертатися до заявника (власника реєстраційного посвідчення) за тел.: (044) 490 3441, факс: (044) 490 3440.